Mimo sukcesów w otrzymywaniu IPSCs, ich dojrzewanie w funkcjonalne kardiomiocyty pozostaje wyzwaniem. Naturalny rozwój kardiomiocytów w organizmie trwa 6-7 lat. Dlatego trwają badania nad przyspieszeniem tego procesu poprzez odpowiednie bodźce fizykochemiczne, takie jak:

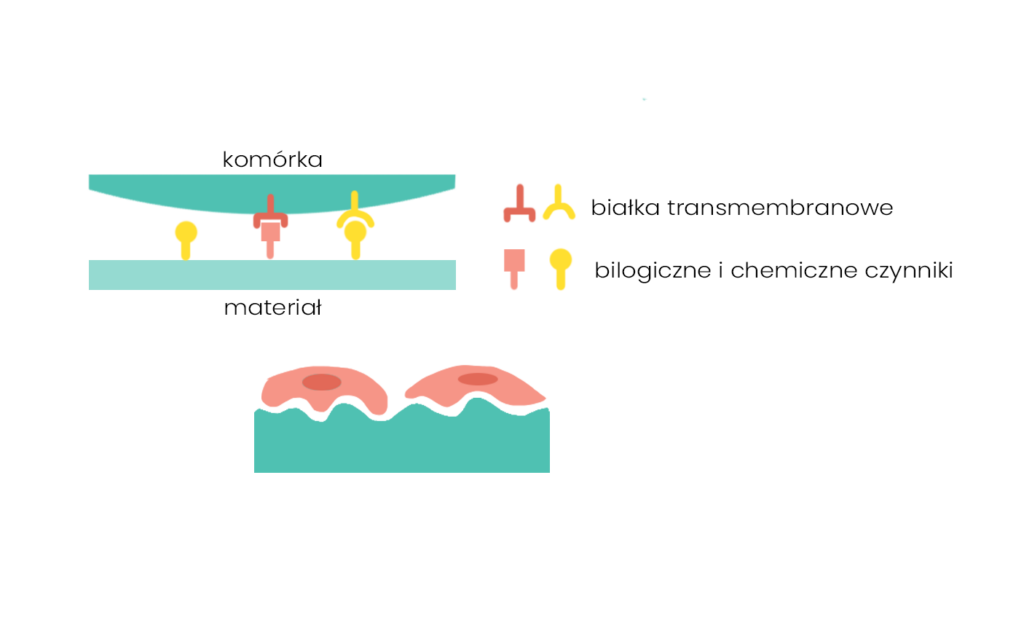
Podłoża biomimetyczne
naśladują strukturę mięśnia sercowego
Stymulacja elektryczna
dla odwzorowania warunków fizjologicznych (pracy komórek rozrusznika serca)
Optymalizacja składu podłoża hodowlanego
wspierającego różnicowanie i dojrzewanie komórek